共计 2593 个字符,预计需要花费 7 分钟才能阅读完成。
帕金森病(Parkinson’s disease, PD)是一种常见于中老年的中枢神经系统退行性疾病,临床上以静止性震颤、运动迟缓、肌强直和姿势平衡为主要特征,其病理表现为黑质致密部多巴胺神经元的损伤和 Lewy 小体的形成。PD 的发病原因非常复杂,其主要病理变化是黑质致密部(SNpc)中多巴胺(DA)能神经元进行性丢失并伴有纹状体多巴胺水平的下降、α- 突触核蛋白(α-synuclein, α-Syn))为主要成分的路易小体的形成,致使得脑部指挥肌肉活动的能力受到不同程度的限制,大大阻碍了患者的活动能力。多巴胺能神经元逐渐丧失会引发许多与帕金森症有关的运动症状。中脑内的特定神经元亚型在帕金森病中尤为脆弱,这凸显了认识其分子和功能多样性的重要性。左旋多巴是广为使用的帕金森症治疗药物,它是多巴胺前体 L-DOPA 的天然形式。
大部分帕金森病患者为散发病例,仅有不到 10% 的患者有家族史,遗传因素、环境因素、衰老、氧化应激等被认为是 PD 的重要诱发原因。PD 研究动物模型应具备以下特征:可以检测到 PD 的行为学异常,随着年龄发展有选择性和渐进性多巴胺神经元损伤,有 Lewy 小体形成。但是帕金森病症状的复杂性以及机制的复杂性也导致动物模型的多样性,目前不同的动物模型只能模拟部分的症状。
利用 MPTP(1- 甲基 - 4 苯基 -1,2,3,6- 四氢吡啶)制备 PD 动物模型是使用最多的一种动物模型。而 MPTP 对于神经系统的毒性作用最早并不是在动物而是在吸毒者上发现的。1979-1982 年期间发现一群加利福尼亚年轻人因吸食新型合成海洛因而患上了严重的不可逆的 PD,出现了典型的 PD 症状,并且对于左旋多巴以及 DA 受体激动剂的治疗有效。研究者在这种新型毒品中发现了含有少量的 MPTP。随后在一系列的动物试验中发现了 MPTP 能够导致 PD 的能力,所引起的症状符合临床 PD 的显著临床表现,因此 MPTP 所处理的动物可以作为一种较为理想的 PD 动物模型。MPTP 本身没有神经毒性作用,它诱发 PD 的机制是 MPTP 穿过血脑屏障,作用于神经胶质细胞,产生甲基苯基吡啶离子 MPP+。MPP+ 能够抑制线粒体呼吸功能,产生氧自由基,从而损伤 DA 能神经元,造成细胞数量减少。
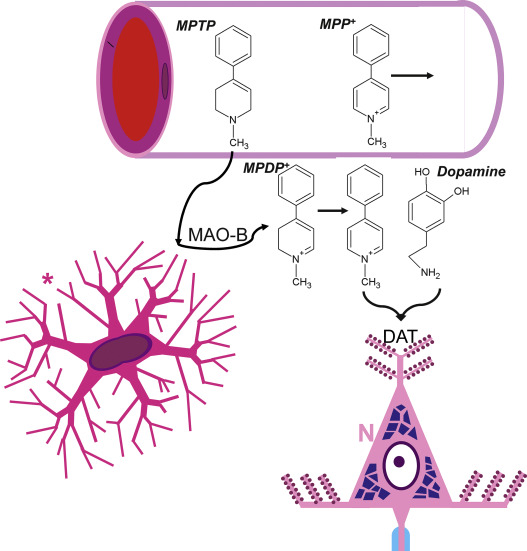
MPTP 是一种常用于建立帕金森病(PD)动物模型的神经毒素,可通过不同给药途径(急性或慢性)诱导疾病样病理。由于其脂溶性,MPTP 能在数分钟内穿过血脑屏障。进入脑内后,MPTP 在神经胶质细胞中被单胺氧化酶 B(MAO-B)代谢为 MPDP+,并进一步自发氧化为有毒的 MPP+。MPP+ 通过有机阳离子转运体(OCT3)释放到脑实质,再经多巴胺转运体(DAT)进入多巴胺能神经元,并在胞质及囊泡中积聚。MPP+ 可抑制线粒体复合体 I,造成 ATP 生成减少、氧化应激增强,最终引起细胞死亡及神经炎症。这一机制为研究 PD 中的多巴胺能神经元退变、线粒体功能障碍及神经炎症提供了重要模型。
灵长类对 MPTP 最敏感但受限制,大鼠和其他造模动物对此神经毒素具有较大的抵抗力,因此常用小鼠进行造模。
MPTP 小鼠模型
MPTP 可在小鼠和灵长类动物(NHP)中建立 PD 模型,但大鼠对 MPTP 不敏感,高剂量则易致死。由于稳定性与可操作性较好,小鼠模型被广泛应用。损伤程度受剂量、注射途径及品系影响。
急性模型:常用腹腔注射(i.p.)单次或短时间多次注射(如每 2 小时注射一次,4 次共 20 mg/kg),可造成纹状体多巴胺减少约 90%、黑质致密部(SNpc)多巴胺神经元减少约 70%,但不形成 α - 突触核蛋白聚集。神经退变在数小时内出现,7 天后稳定。
行为表现:小鼠表现出运动障碍,但可在数天内恢复,限制了行为学研究持续时间。神经退行和恢复程度与遗传背景(品系)有关。
肠道菌群研究:MPTP 模型也用于研究 PD 中的肠道菌群失衡。来自 MPTP 处理小鼠的粪菌移植可降低多巴胺水平并诱发运动障碍,而正常菌群移植可缓解症状。
亚急性 / 慢性模型:连续多日给予低剂量 MPTP 可诱导渐进性黑质—纹状体神经退变及 α - 突触核蛋白积聚,更接近 PD 慢性进展特征,但运动障碍不明显。
MPTP 灵长类模型(NHP)
在非人灵长类中,MPTP 是 PD 研究的金标准模型。
诱导方式:多为多次低剂量系统性注射(1–2 mg/kg),或单侧颈动脉注射形成偏侧帕金森综合征。症状通常在数月内形成,并可维持数月。
慢性模型:每日 0.2 mg/kg 注射 2–3 周,可模拟 PD 早期的渐进性神经元丧失。灵长类动物的运动功能可能在数月后部分恢复,可再次给予 MPTP 延长实验周期。
病理与症状:MPTP 在灵长类中诱导的多巴胺能神经元损伤与 α - 突触核蛋白聚集,与人类 PD 非常相似。损伤严重程度决定运动障碍的程度。症状包括震颤、嗅觉丧失、睡眠障碍等,L-DOPA 治疗可暂时改善运动功能,但长期使用会出现异动症。
造模方法:
在注射当天配制好新鲜的 MPTP 溶液,然后腹腔或皮下注射 MPTP。试剂要现用现配。
根据实验要求和目的,可分为快速模型和慢速模型。
快速模型可分为单次注射和多次注射。单次注射的剂为 30mg/kg,该模型损伤轻,易恢复;多次注射的剂量为 20mg/kg,每隔 2h 注射 1 次,共 3 - 4 次,该模型损伤快且严重,DA 神经元的损伤到死亡可以在 3d 内完成。
慢速模型需多次注射,每天 1 次,单次注射的剂量为 20mg/kg, 连续注射 5 -7d。该模型的成活率较高,实验周期较长。
模型验证:
(1)造模后进行行为学观察参照 Francois 的实验方法 (包括行动迟缓实验、抓握实验和尾强直实验记录强直症状的变化、震颤实验) 记录帕金森氏病的三大症状,观察到小鼠出现尾巴僵硬竖直,身体出现非自主性震颤,自发活动减少,表明帕金森模型构建成功。
(2)离体脑组织中黑质、纹状体免疫组化染色
MPTP 在注射后,7d 对小鼠黑质致密部(SNpc)和纹状体(Striatum)免疫染色。结果所示,在进行造模后,小鼠纹状体(Striatum)末端和黑质致密部(SNpc)的酪氨酸羟化酶 (TH) 阳性细胞体和纤维所形成的的网状结构密度显著降低,且 TH 阳性细胞数量显著降低,TH 阳性纤维密度显著降低。
MPTP 通过模拟线粒体功能障碍与多巴胺能神经元退行性损伤,在小鼠与灵长类动物中成功重现了 PD 的主要病理特征。小鼠模型适用于研究机制与早期筛药。灵长类模型则因其更接近人类 PD 的行为与病理特征,被用于临床前药物、基因治疗及神经刺激等研究。
