共计 1673 个字符,预计需要花费 5 分钟才能阅读完成。
诱导多能干细胞(iPSC)是通过将成熟体细胞(如皮肤或血细胞)导入特定转录因子重编程而获得的多能干细胞,具有与胚胎干细胞相似的分化潜能。胚胎干细胞(ESC)则来源于早期囊胚的内细胞团,是天然存在的多能细胞系。ESC 能无限增殖并分化为三胚层各类细胞,但其来源涉及胚胎伦理问题而受限。iPSC 的出现绕过了胚胎伦理争议,可在体外从患者自身或供体细胞获得多能干细胞(具有个性化和低免疫原性的优势)。
近年研究和注册的临床试验显示,两者均用于组织修复和疾病治疗研究。iPSC 相关临床试验已超过 160 项,主要集中在神经系统疾病、心血管疾病、代谢疾病、眼科疾病和肿瘤等领域。例如,澳大利亚 Cynata 公司开发的骨关节炎 iPSC 衍生间充质细胞产品 CYP-004,已进入Ⅲ期临床。ESC 相关临床试验也在多种适应症开展,包括年龄相关性黄斑变性(通过 ESC 分化的视网膜色素上皮细胞移植)、1 型糖尿病(ESC 分化的胰腺祖细胞)以及帕金森病、脊髓损伤、缺血性心脏病等。
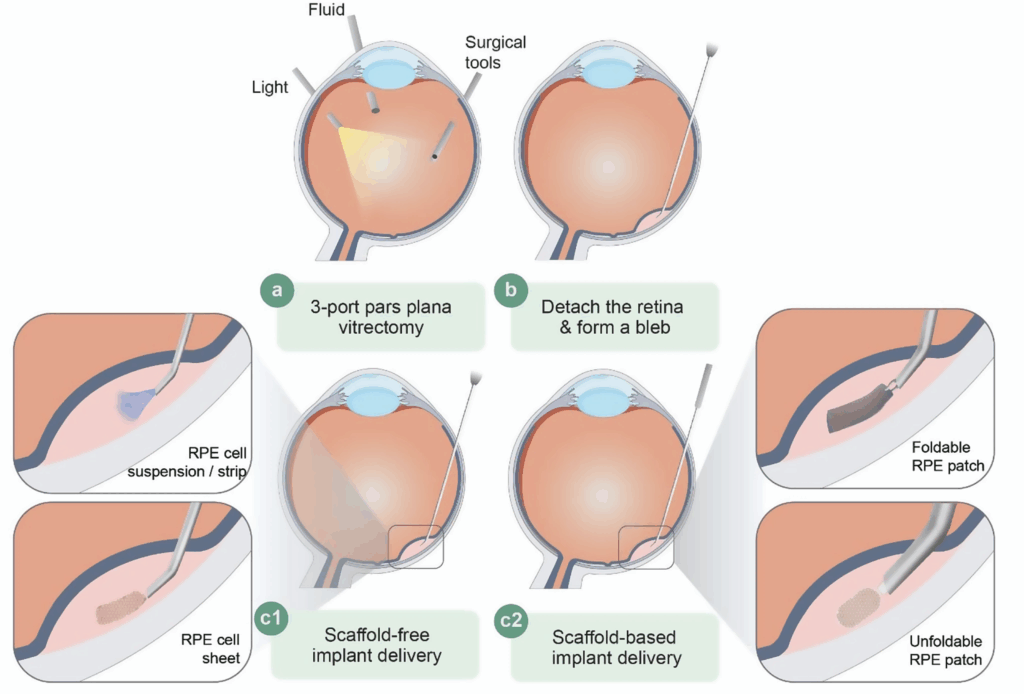
图 1:正常视网膜组织与退化视网膜及基于 PSC 的视网膜色素上皮(RPE)细胞移植示意。
已有多项临床研究利用 ESC 或 iPSC 来源的 RPE 细胞治疗黄斑变性。Schwartz 等的Ⅰ期试验报告,在黄斑变性患者中使用 hESC 来源 RPE 细胞,2 年随访未见严重不良事件。日本研究团队将自体 iPSC 来源的 RPE 细胞片移植到一名湿性 AMD 患者体内,术后 4 年视力保持稳定,未发生排斥或严重不良反应。类似地,iPSC 技术也正应用于其他组织修复。例如,日本首次人体试验将 iPSC 来源的心肌细胞贴片移植于缺血性心肌病患者,1 年内未出现细胞相关不良事件且部分患者心功能有所改善,提示 iPSC 心肌疗法具有良好的安全性潜力。
安全性问题
-
基因组稳定性 :iPSC 制备和扩增过程中可能发生基因突变,需要通过核型分析、全基因组测序等手段严格监控。
-
致瘤性 :未分化的 iPSC 或 ESC 具有形成畸胎瘤的潜力。临床应用中,一旦残留少量未分化多能细胞,移植后可在体内发育成肿瘤(曾有病例报告 iPSC 治疗后患者皮下出现携带多能性标志物的肿块)。因此,需要通过纯化分化细胞和预处理措施去除未分化细胞。
-
免疫排斥 :ESC 衍生移植物属于异体移植,往往需应用长期免疫抑制剂以防排斥;相比之下,自体 iPSC 因其低免疫原性可显著降低排斥风险(曾有 nAMD 患者接受自体 iPSC-RPE 移植未用抑制剂且无排斥反应)。然而,异体 iPSC(如同种异体)仍需注意免疫监控。
-
异质性 :不同来源或重编程方法生成的 iPSC 株间可能存在表观遗传和分化效率差异,影响治疗一致性,这也是当前需解决的挑战之一。
优势与限制
-
iPSC 优势 :无需使用胚胎资源,伦理接受度高;可制备个性化细胞(降低免疫排斥);易于进行基因修复和疾病模型构建,在再生医学和个性化医疗中应用前景广阔。
-
iPSC 局限 :重编程效率和纯度仍需优化;潜在基因组异常和表观遗传记忆风险;体外分化成熟度通常低于体内环境,产品生产成本高。
-
ESC 优势 :作为多能干细胞研究的“金标准”,其分化体系成熟且稳定,可高效获得所需细胞类型。在某些实验和临床研究中显示出强大的治疗潜能。
-
ESC 局限 :获取 ESC 需破坏胚胎,存在严重伦理争议;移植为异体细胞,需长期免疫抑制,排斥风险高;细胞来源有限,难以满足大规模治疗需求。
最新研究成果与未来趋势
当前研究聚焦于提高安全性和适用性:采用 mRNA、无病毒载体或小分子重编程等无插入方法,降低重编程过程中插入突变的风险;通过细胞表面标记物纯化或药物诱导凋亡等策略剔除残留未分化细胞以减少致瘤性。基因编辑技术(CRISPR/Cas9)正在应用于纠正疾病相关突变并构建通用供体细胞株。例如,可敲除 iPSC 的 HLA I/II 基因并引入 PD-L1 等免疫调节蛋白,以创建无需免疫抑制剂的“低免疫原性”细胞库。此外,iPSC 驱动的类器官和体外疾病模型技术正在加速发展,为新药筛选和机理研究提供平台。未来,随着干细胞生产工艺和质量控制标准的完善,预计更多基于 iPSC 和 ESC 的细胞疗法将进入后期临床试验,并向规模化、规范化、个性化方向发展。
